


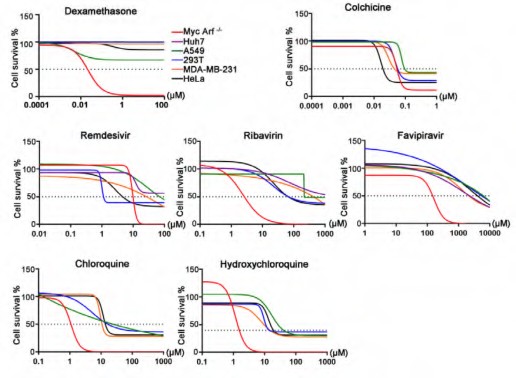
Для борьбы с инфекцией SARS-CoV-2 широко используются несколько препаратов, включая дексаметазон и колхицин для подавления чрезмерного иммунного ответа; противовирусные препараты ремдесивир, фавипиравир и рибавирин; и противомалярийные препараты хлорохинфосфат и гидроксихлорохин для комбинированного подавления репликации вируса и иммунного ответа. Однако в настоящее время мало что известно о генетических биомаркерах, которые могут повлиять на эффективность этих препаратов.
Команда ученых из Университет Китайской Академии наук представила первый отчет о CRISPR-скрининге этих препаратов для лечения COVID-19 по всему геному с данными как о механизмах устойчивости, так и о механизмах сенсибилизации. Ученые разработали метод скрининга, который использует общегеномные библиотеки sgRNA для систематического выявления генов, критически важных для действия этих препаратов. Они обнаружили гены, имеющие решающее значение для импорта, экспорта, метаболической активации и инактивации ремдесивира, а также гены, которые регулируют иммуносупрессивные эффекты колхицина и дексаметазона. Их результаты показывают, что группа генов, участвующих в аутофагии, а также в синтезе липидов и холестерина, существенно модулирует действие хлорохиновых препаратов. Многочисленные клинические исследования показали, что клинический результат противоопухолевых препаратов на основе нуклеозидов, структурно сходных с противовирусными препаратами, определяется статусом экспрессии их соответствующих переносчиков и метаболизирующих ферментов.
При воздействии колхицина наиболее высоко экспрессировались гены TMEM161B и POU2F1, связанные с устойчивостью к другим лекарственным средствам, дестабилизирующим микротрубочки. Если пациент страдает дефицитом этих генов, колхицин неспособен в достаточной степени подавлять иммунный ответ. Фавипиравир является противовирусным пролекарством и, следовательно, требует обширного метаболического превращения in vivo перед эффективным проникновением в клетку-мишень. В этом исследовании было отмечено, что только гены гибели клеток были значительно обогащены в выжившей популяции, в то время как некоторые механизмы инактивации лекарств были исчерпаны. Что касается механизмов транспорта и инактивации лекарств, группа отметила, что клетки, выжившие после воздействия испытуемых препаратов, часто имеют повышенную регуляцию молекулярных насосов выведения лекарств, специфичных для конкретного препарата. Ремдесивир лучше всего удалялся из клеток, экспрессирующих ABCC1, тогда как колхицин наиболее эффективно удалялся ABCC1 и ABCB1. Было также отмечено, что высокая экспрессия гена нуклеотидазы NT5C2 значительно снижает цитотоксичность ремдеcивира и фавипиравира, инактивируя их.
Результаты работы предоставляют предварительную информацию для разработки генетических биомаркеров для мониторинга эффективности лечения. Такие биомаркеры помогут лучше интерпретировать данные клинических испытаний лекарств от COVID-19 и укажут подходы к стратификации пациентов с COVID-19 для правильного лечения этими препаратами.