


Пигментный ретинит или врожденный амавроз Лебера (LCA) впервые описанный в 1867 году Теодором Лебером, представляет собой клинически и генетически гетерогенную группу заболеваний – дистрофий сетчатки детского возраста. Он поражает примерно 1 из 40 000 новорожденных. Это заболевание, в зависимости от молекулярной природы, может наследоваться и связано с мутациями в ядерной ДНК. Его не стоит путать с наследственной оптической нейропатией Лебера, которая связана с мутациями в митохондриальной ДНК. Мутации в пигментном эпителии сетчатки (RPE) 65 связаны с LCA, для которого не существует эффективной терапии, снижающей прогрессирующую дегенерацию сетчатки у пораженных пациентов.
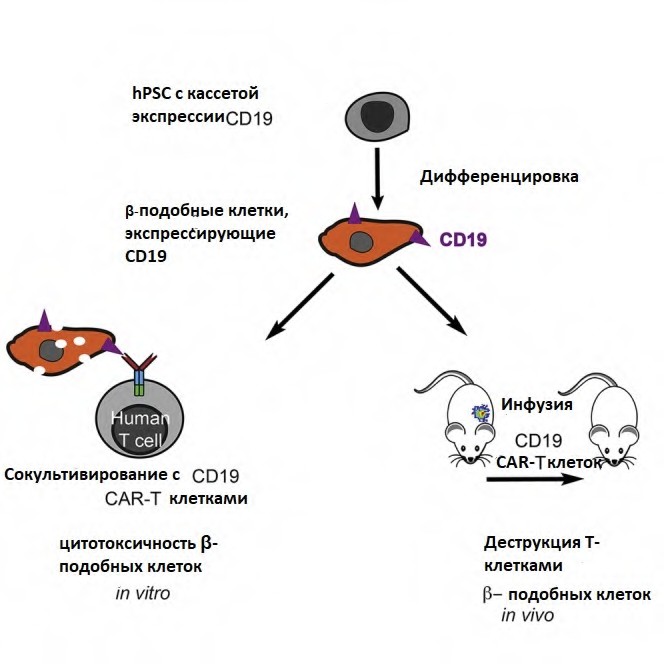
Аутоиммунное разрушение β-клеток поджелудочной железы лежит в основе патогенеза диабета 1-го типа. Большинство локусов, ассоциированных с риском развития сахарного диабета 1-го типа, имеют отношение к генам, активным в T-клетках, что позволяет предположить, что T-клетки принимают активное участие в развитии этого заболевания. Поэтому понимание механизмов, лежащих в основе взаимодействия β-клеток поджелудочной железы и аутореактивных Т-лимфоцитов является крайне важным в борьбе с диабетом 1-го типа.
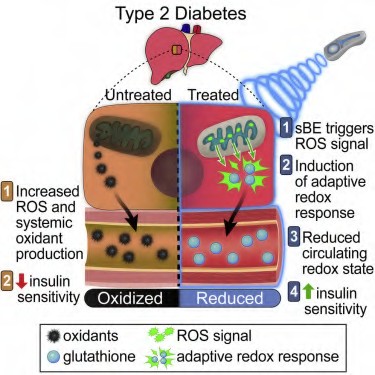
Исследователи из Университета Айовы (США) обнаружили новый безопасный способ неинвазивного контроля уровня сахара в крови. Согласно полученным результатам, воздействие на мышей с диабетом комбинацией статических электрических и магнитных полей в течение нескольких часов в день нормализует два основных признака сахарного диабета 2 типа.
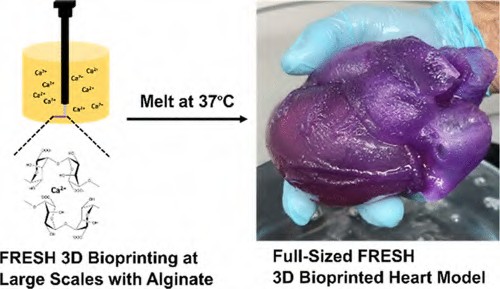
Профессор биомедицинской инженерии Адам Файнберг и его команда из университета Питтсбурга (США), используя технику Freeform Reversible Embedding of Suspended Hydrogels (FRESH), создали первую полноразмерную трехмерную модель человеческого сердца посредством биопечати.
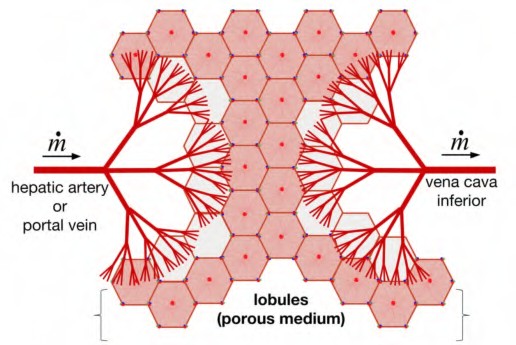
Существующие модели кровообращения печени варьируются от полноразмерных, представляющих целостную архитектуру кровообращения до микроциркуляторных. Виртуальные сети печени сочетают биологию с механикой жидкости и массопереносом в качестве нового подхода к физиологическим моделям. Однако эти модели, независимо от их уровня сложности, носят описательный характер. Отсутствует подход, который позволил бы предсказать архитектуру потока печеночного кровообращения: трансплантация или резекция печени с целью лечения опухолей печени может привести к печеночной недостаточности с катастрофическими последствиями, в случае отсутствия контроля за артериальным давлением.