Статья размещена в открытом доступе и распространяется на условиях лицензии Creative Commons Attribution (CC BY).
МЕТОД
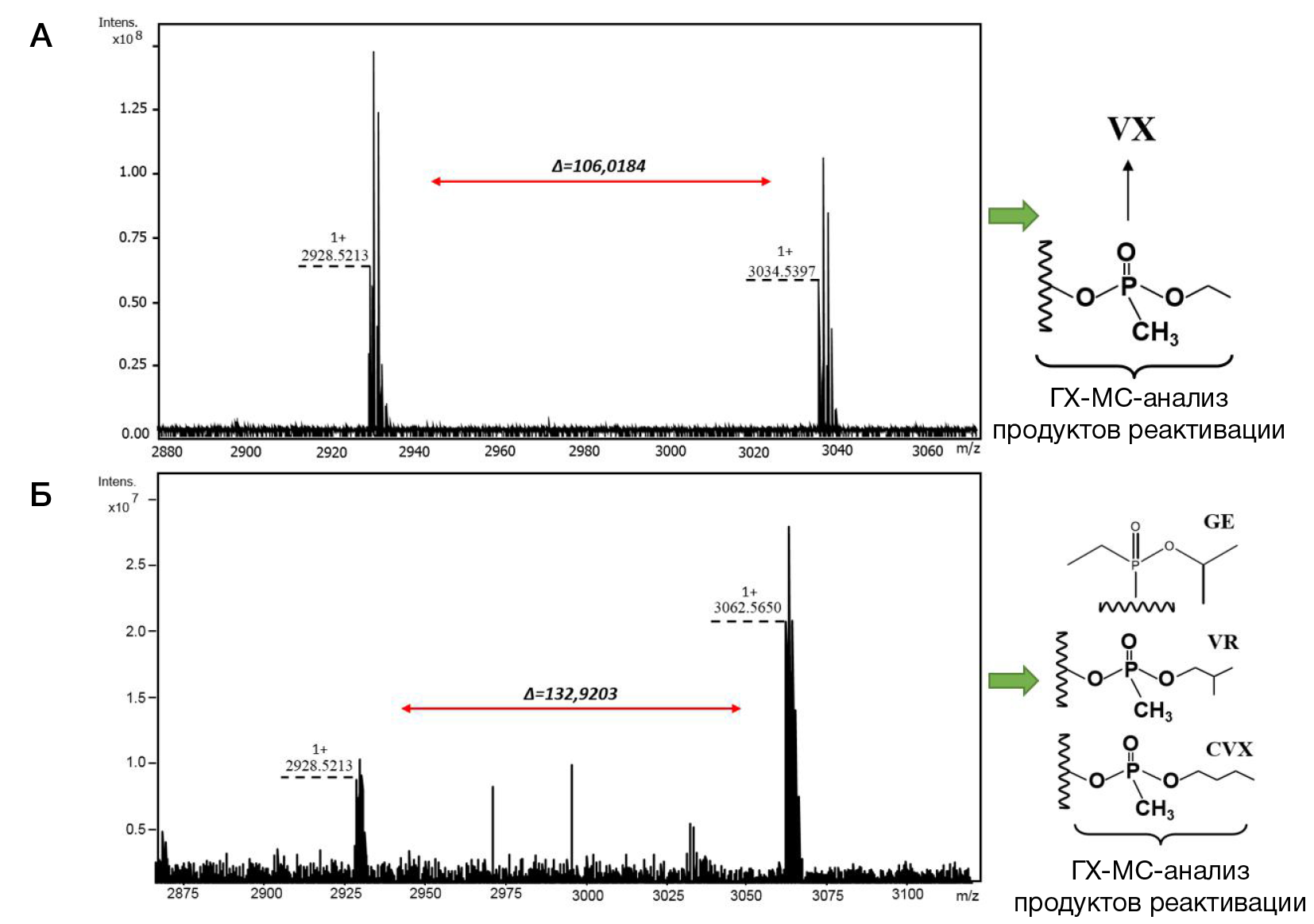
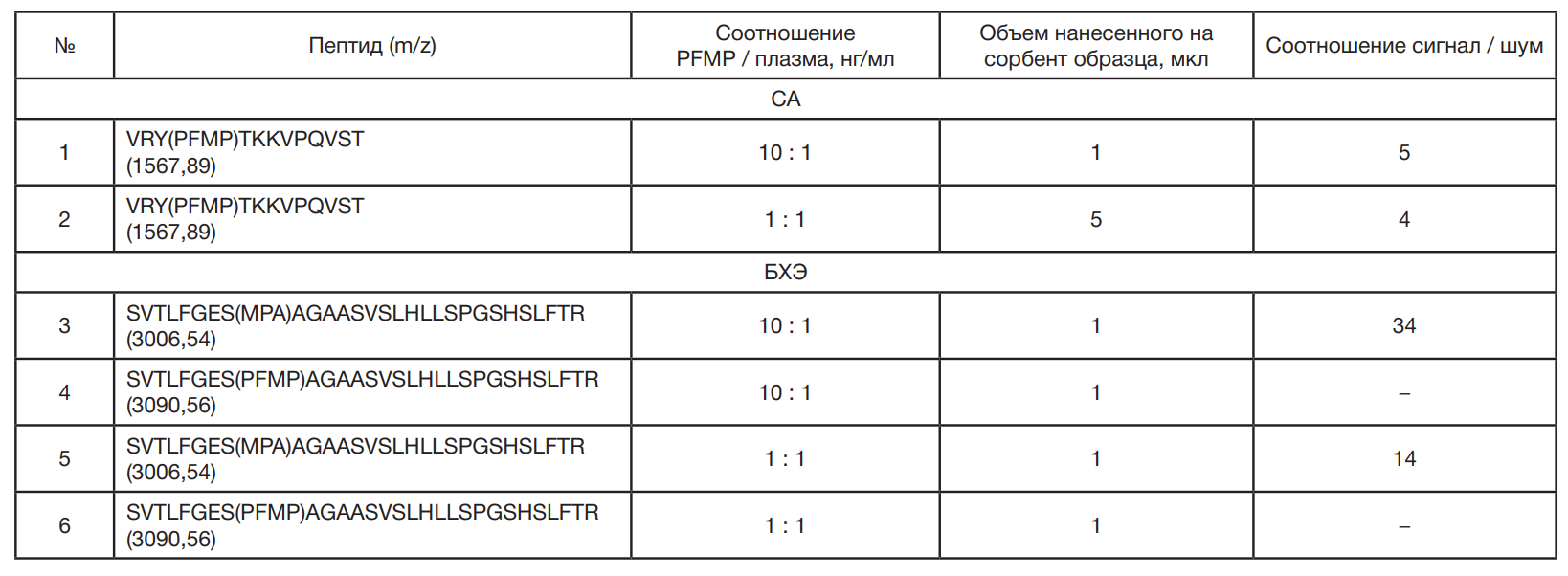
Идентификация фосфонилированных пептидов с применением МАЛДИ-мишени, функционализированной стеаратом лантана
1 Научно-исследовательский институт гигиены, профпатологии и экологии человека Федерального медико-биологического агентства, Санкт-Петербург, Россия
2 Научно-клинический центр токсикологии имени С. Н. Голикова Федерального медико-биологического агентства, Санкт-Петербург, Россия
3 Институт аналитического приборостроения Российской академии наук, Санкт-Петербург, Россия
4 Санкт-Петербургский государственный университет, Санкт-Петербург, Россия
Для корреспонденции: Владимир Николаевич Бабаков
г.п. Кузьмоловский, ст. Капитолово, корп. 93, Ленинградская обл, Россия; ur.hcepg@vokabab
Благодарности: авторы выражают благодарность за техническую поддержку ресурсным центрам «Развитие молекулярных и клеточных технологий» и «Геомодель» Научного парка СПбГУ, а также А. А. Селютину за возможность работы с МАЛДИ масс-спектрометрическим оборудованием.